16.07.2020
16.07.2020 Шановні колеги!
Пропонуємо Вашій увазі дослідження компанії Angelantoni Life science S.r.l., ІТАЛІЯ, у використанні плазми пацієнтів, які виробили специфічні антитіла проти SARS-CoV-2 інфекції.
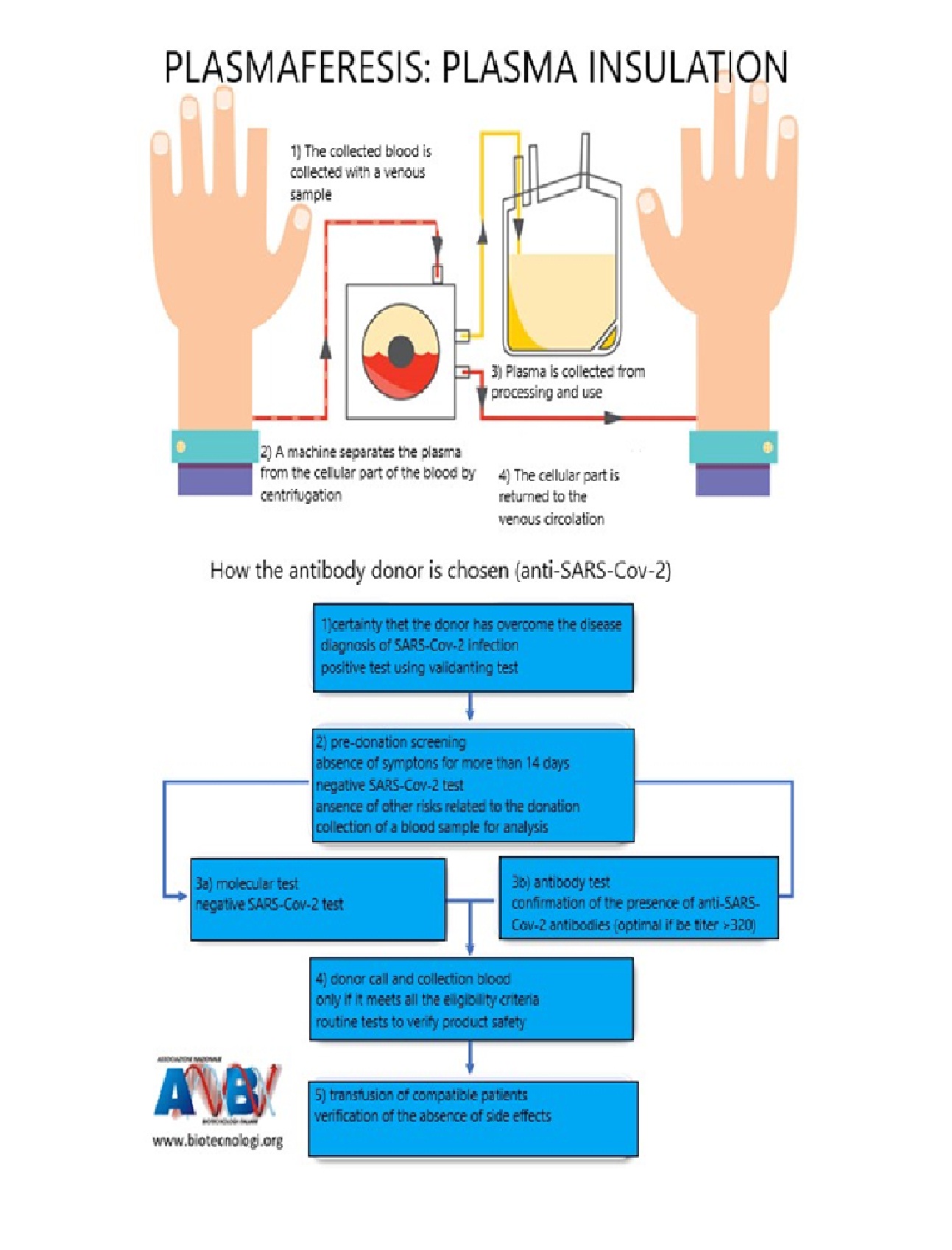
ПЛАЗМАФЕРЕЗ: ВІДОКРЕМЛЕННЯ ПЛАЗМИ
У цій статті ми спробуємо пояснити застосування цієї терапевтичної процедури, яка відома світовій медицині вже приблизно 100 років та використовувалась у 2013 для боротьби з єпідемією Ебола, а також яким чином Angelantoni Life Science може активно реагувати на сучасні виклики, пропонуючи важливий внесок у пошук ефективної терапевтичної стратегії.
Було продемонстровано, що призначення плазми пацєнтів, які «одужали» або імуноглобулінів веде до зменшення часу знаходження у лікарні, а також зниження рівня смертності пацієнтів з COVID-19. Інтерлейкіни 6, 10 (інтерлейкіни це фактори, що призводять до розвитку гострого запалення) та фактор некрозу пухлини- альфа були прийняті в якості «контрольних рівнів». Призначення важким пацієнтам фракціонованої плазми (H1N1), а згодом збагаченої іммуноглобуліном Ig (H-IVIG), веде до значного зниження вірусного навантаження через 5 днів
Специфічні IgG-антитіла до SARS-CoV-2, що пасивно передаються через перелиту плазму, активно впливають на імунну систему пацієнта-реципієнта нейтралізуючи вірусні частинки та активуючи систему комплементу, сприяючи тим самим елімінації вірусу. Проте, важливо також усвідомлювати, що переливання плазми може асоціюватися з несприятливими трансфузійними реакціями, такими як алергічна реакція, гостре посттрансфузійне пошкодження легень (TRALI) і циркуляторне перевантаження.
Після інфузії плазми від людей, які одужали, пацієнти демонструють кращу оксигенацію та зниження маркерів запалення на рентгенограмах, а також зменшення вірусного навантаження. При використанні плазми для лікуваня реакція нейтралізації рекомендована в якості оптимального тесту для оцінювання відповідного донора або плазми. Проте, деякі дослідження зразків, отриманих у пацієнтів, які захворіли двосторонньою пневмонією під час COVID-19, показали, що IgG при ІФА добре корелює з титрами нейтралізації у випадках MERS, тому це може бути відповідним скринінговим тестом для донорства плазми.
Научні докази недостатні через відсутність широкомасштабных клінічних досліджень, які могли б бути репрезентативними для цільових популяцій. По друге, кількість антитіл, які призначаються кожному пацієнту, не стандартизирована. Нарешті, плазма донорів, що одужали, зазвичай призначається з іншим лікуванням, як наприклад, противірусні препарати і кортикостероїди, що може впливати на взаємодію плазми та антитіла, плутаючи результати.
Незважаючи на обмеження, наші випадки свідчать, що плазма пацієнтів, які одужали від COVID-19 інфекції може бути додатковою можливістю для лікування пацієнтів, не викликаючи серйозних побічних ефектів. При застосуванні у поєднанні з кортикостероїдами системної дії також було підтверджено зниження надмірної запальної реакції пацієнта та зменшення вірусного навантаження. Необхідні подальші добре розроблені дослідження, щоб продемонструвати ефективність та безпеку переливання гіперімунної плазми пацієнтам з COVID-19.
Що ми знаємо: Імуноглобулін (IG), отриманий з плазми людини, використовується для лікування, щоб забезпечити рівень захисних антитіл у пацієнтів з первинним імунодефіцитом (ПІД) та для профілактики інфекційних хвороб. Для визначення амплітуди необхідних для клінічного ефекту антитіл важливо розуміти регіональні особливості поширеності сироваткових антитіл у плазмі, з якої виготовляється продукція IG (епідеміологічні дослідження).
Завдяки раціональному підходу, що поєднує епідеміологічний нагляд і стратегічне управління ланцюгом поставок плазми, проведення лікування гіперімунною сироваткою, збагаченою IgG, може бути більш ефективним та економічним ніж сліпий скринінг або методи імунізації. Принаймні, виробники GI можуть спробувати усвідомити регіональні відмінності ефективності антитіл, які виробились в результаті природного імунітету порівняно з імунізацією. У глобальному масштабі регіональні поставки мають потенціал, щоб бути внутрішнім захистом першої лінії проти інфекційних хвороб, що виникають у різних частинах світу. Незалежно від особливостей, дієвість цієї стратегії буде залежати від функціонального набору антитіл з різних площадок для збирання плазми.
В останні тижні вчені пристосувались використовувати фракційне переливання плазми або гіперімунних імуноглобулінів в якості альтернативної терапії для лікування пандемії, доки очікується потенційна та остаточна вакцина. FDA затвердила використання трансфузій «сироватки» в якості пасивної терапії антитілами за умови, що кожен заклад відповідає всім вимогам безпеки: доступність та скринінг донорів, які вилікувались від COVID-19, добре розроблені протоколи досліджень для забезпечення аналізу ефективності таких втручань; урядові та інституційні узгодження і підтримка лабораторій для проведення серологічного та молекулярного тестування, включаючи проведення реакцій нейтралізації вірусу та імунної відповіді. Оскільки дози гіперімунної або збагаченої плазми можуть бути заморожені перед розподіленням, зв'язок між лікарнями, центрами крові і виробництвом плазми повинен здійснюватись бездоганно.
Необхідність працювати з біологічними матеріалами, по суті, має неодмінну потребу зберігати продукцію незміненою, незалежно від того, готова вона чи знаходиться в процесі виготовлення. Лише за низьких температур ми можемо сповільнити хіміко-фізичні реакції, які руйнують біологічну субстанцію
Angelantoni Life Science може запропонувати корисні рішення для вирішення проблем консервації. Для цього процесу ми представляємо функціональне обладнання Медичних Пристроїв IIa класу, сертифікованих згідно Директиви 93/42. Плазма ПОВИННА бути заморожена для адекватного збереження важливих для процесу коагуляції лабільних факторів, які вона містить, таких як фактор VIII. Цей етап виконує Рекомендації R (95) 15 ЕС, які вимагають від нас досягнення температури -30°C в центрі контейнера менше, ніж за 60 хвилин. У зв’язку з цим ми хотіли б підкреслити, що всі моделі можуть забезпечити ефективність та однорідність заморожування, про які йдеться в Рекомендаціях. Необхідність отримувати якомога більший об’єм даних для валідації процесу перетворюється на все більш масивний відбір зразків і аналіз циклів, отже збирання все більшої кількості зразків є неминучим. Всі зразки повинні тимчасово зберігатись саме через вищевказані проблеми.
Більше інформації про заморожувачі плазми наведено у нашому каталозі.